Densidade eletrônica e distribuição de carga em uma molécula¶
A estrutura eletrônica de uma molécula pode ser calculada pelas equações da mecânica quântica. Entretanto, aqui não consideramos os elétrons explicitamente. Em nosso tratamento pela teoria de forças intermoleculares, a densidade eletrônica de uma molécula é combinada à carga dos prótons dos núcleos atômicos, e o resultado é a distribuição de carga da molécula.
A figura abaixo mostra a molécula de etanol (CH$_3$CH$_2$OH). No lado esquerdo, temos uma superfície da molécula, colorida de acordo com sua distribuição de carga: vermelho nas regiões negativas (ou seja, onde a densidade de elétrons é maior que a carga dos prótons naquela região), verde em regiões neutras (onde a densidade dos elétrons e dos prótons se cancelam) e azul em regiões positivas (onde a densidade eletrônica é menor que a carga dos prótons).
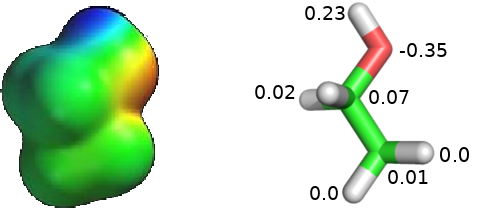
No lado direito da figura, temos na mesma orientação uma representação de bastões do etanol colorida segundo o átomo (H branco, O vermelho e C verde). A distribuição de carga em uma determinada região da molécula pode ser condensada sobre seus centros atômicos, resultando em cargas parciais ($q_i$) com valores mostrados na figura (em unidades de carga eletrônica, $|e|$).
Note que a distribuição de cargas nas duas representações está de acordo com a eletronegatividade dos átomos (maior no oxigênio) e que a soma das cargas parciais equivale à carga total da molécula (neutra, neste exemplo do etanol).
Distribuição de carga em multipolos ¶
A distribuição de carga de uma molécula também pode ser descrita por uma expansão multipolar. Assim como uma série de Taylor, apenas os primeiros termos são necessários para uma boa descrição da distribuição.
Para uma molécula carregada, o primeiro termo da expansão é o momento monopolo, uma carga pontual no centro da molécula com valor equivalente a sua carga total. Para uma molécula neutra e polar, o monopolo é nulo, mas o segundo termo da expansão, o momento de dipolo $\vec{\mu}$, já provém uma boa descrição da distribuição. Por exemplo, a distribuição de carga da molécula de água é bem descrita pelo seu dipolo $\vec{\mu}_{H_2O}$, cujo módulo medido experimentalmente é $|\vec{\mu}_{H_2O}|=1.85$ debye (D).
As diferentes descrições da distribuição de carga de uma molécula são compatíveis. Veja abaixo dois exemplos para as moléculas de água (H$_2$O) e de amônia (NH$_3$). O controle vertical altera o valor da carga parcial $\delta$ condensada em cada um dos átomos de hidrogênio. Observe o vetor que representa o momento de dipolo, com origem no centro de massa da molécula. Seu módulo $|\vec{\mu}|$ e magnitude variam de acordo com o valor da carga parcial $\delta$:
Devido à simetria da molécula de água, a carga parcial de cada um dos seus hidrogênios ($\delta$) é igual. O mesmo vale para amônia. Mas, note que o valor de $\delta$ é diferente em cada molécula. Como H$_2$O e NH$_3$ são neutras, a carga parcial do oxigênio na água é $q_O = -2\delta$ e a carga parcial do nitrogênio na amônia é $q_N = -3\delta$.
Pergunta: Qual valor de carga parcial $\delta$ é compatível ao dipolo experimental da água (veja seu valor acima)? E para reproduzir o dipolo da amônia, $|\vec{\mu}_{NH_3}|=1.43$ D?
Resposta de polarização da densidade eletrônica ¶
Até aqui consideramos apena uma molécula isolada e analisamos sua distribuição de carga intrínseca ou estática. Mas o que acontece quando uma molécula interage com outra partícula? A densidade eletrônica desta molécula responderá à interação e sofrerá uma distorção, ou uma polarização conforme o termo mais usado. Esta resposta dependerá da polarizabilidade $\alpha$ da molécula.
Imagine primeiro uma partícula colocada em um campo elétrico $\vec{E}$, criado por duas placas paralelas com carga oposta. Aqui vamos assumir que $\alpha$ é isotrópica, ou seja, a polarizabilidade não depende da direção do campo elétrico aplicado. Veja abaixo dois exemplos pictóricos para partículas com núvem eletrônica colorida em azul ou rosa e, respectivamente, polarizabilidade $\alpha_1$ e $\alpha_2$. Altere a intensidade do campo elétrico usando o controle horizontal, e observe a distorção da densidade eletrônica e a criação de um vetor de dipolo induzido $\vec{\mu}_{ind}$:
Enquanto o campo elétrico esta desligado, $\vec{E}=\vec{0}$, ambas partículas tem nuvens esféricas e são apolares. Em resposta ao campo, a nuvem distorce e a densidade eletrônica aumenta perto da placa positiva e diminui perto da placa negativa. Assim, a distribuição de carga é polarizada e um dipolo é induzido na partícula $i$, segundo a equação:
$$\vec{\mu}_{ind, i} = \alpha_i \vec{E}$$
No exemplo acima, a polarizabilidade da partícula rosa é maior, $\alpha_2 > \alpha_1$. Logo, o módulo do dipolo induzido nesta partícula será maior do que na partícula azul, $|\vec{\mu}_{ind,2}| > |\vec{\mu}_{ind,1}|$, para a mesma intensidade de campo elétrico aplicado. Dizemos que a densidade eletrônica da partícula rosa é mais "mole", ou que a azul é mais "dura".
A situação é similar quando, ao invés de placas de carga oposta, temos duas partículas interagindo. Veja abaixo dois exemplos em que a partícula azul interage com um íon ou com uma molécula com dipolo permanente $\vec{\mu}_{perm}$. Aproxime as duas partículas com o controle horizontal e observe a resposta de polarização:
A interação das partículas separas é praticamente nula. A medida que o cátion aproxima-se, seu campo elétrico atrai os elétrons e induz um dipolo $\vec{\mu}_{ind}$ na partícula azul. Quando aproxima-se a molécula com dipolo permanete, colorida em vinho, novamente a nuvem eletrônica na partícula azul é polarizada e um dipolo é induzido, mas desta vez em sentido oposto ao exemplo anterior e paralelo ao dipolo permanente $\vec{\mu}_{perm}$. Note que o dipolo induzido na partícula azul também possui um campo elétrico cuja resposta da nuvem eletrônica na molécula vinho induz um aumento do seu dipolo. Este efeito é desprezível para o cátion, pois sua nuvem eletrônica é muito mais dura.
Finalmente, temos a situação em que duas partículas apolares interagem. Veja abaixo o comportamento das núvens eletrônicas quando as partículas são aproximadas:
Mesmo na ausência de um campo elétrico permanente, dipolos instantâneos $\vec{\mu}_{inst}$ são produzidos quando as partículas se aproximam. Este efeito tem origem na correlação da movimentação dos elétrons quando as duas partículas são aproximadas e resulta na contribuição dispersiva da interação de van der Waals. Nas próximas notas, veremos equações simples que descrevem energias potenciais das interações entre cargas parciais e respostas de polarização em moléculas como descrito acima.